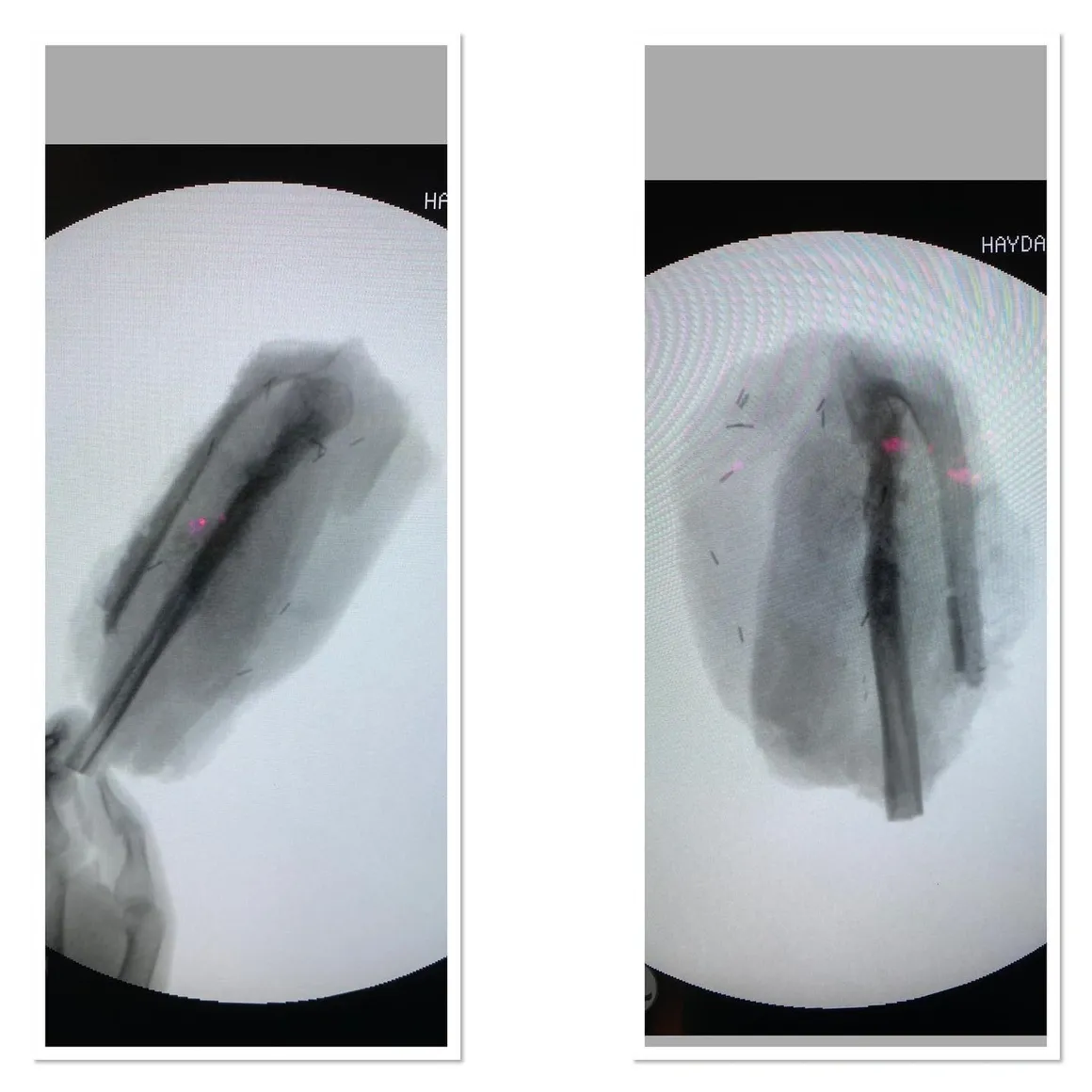
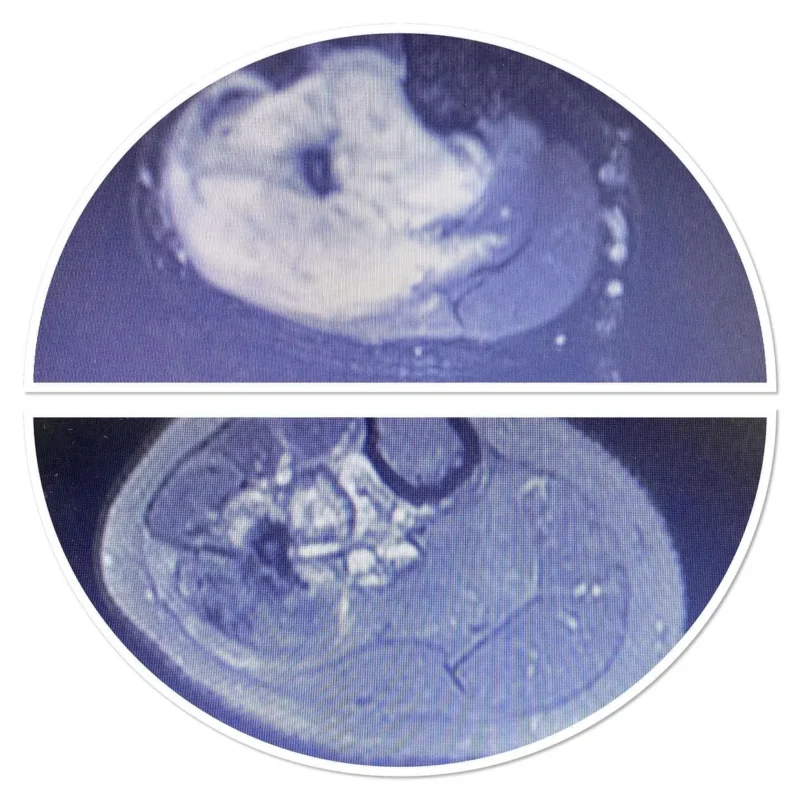
Опухоли костей
Соответствующее и эффективное исследование опухолей костей хирургом-ортопедом с его командой (рентгенолог-ортопед, патолог-ортопед, сосудистый хирург, микрохирург с достаточным опытом реконструкции, онколог-радиолог и онколог) имеет важное значение для адекватного лечения пациента, в противном случае лечение пациента будет неправильным. Диагностика или задержка диагностики приведет к серьезным нарушениям и смерти.
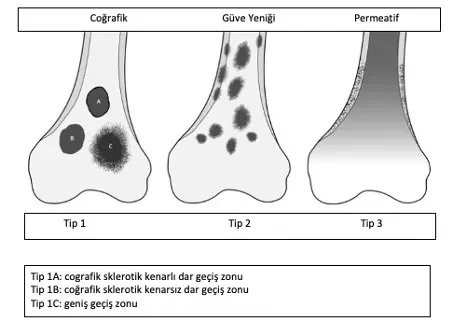
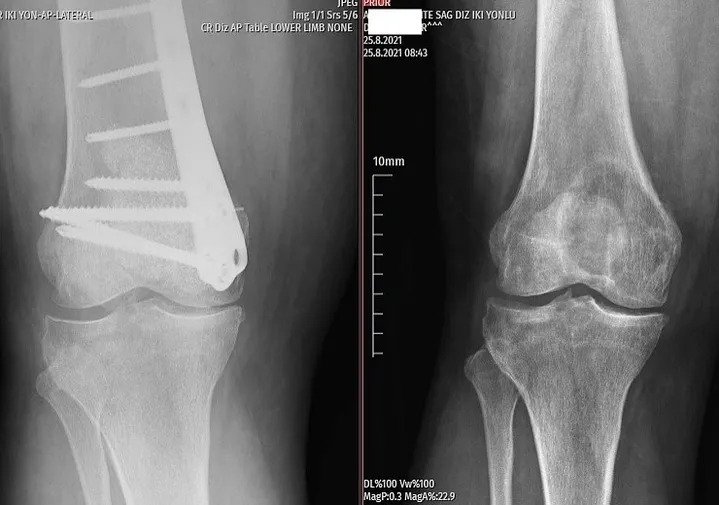
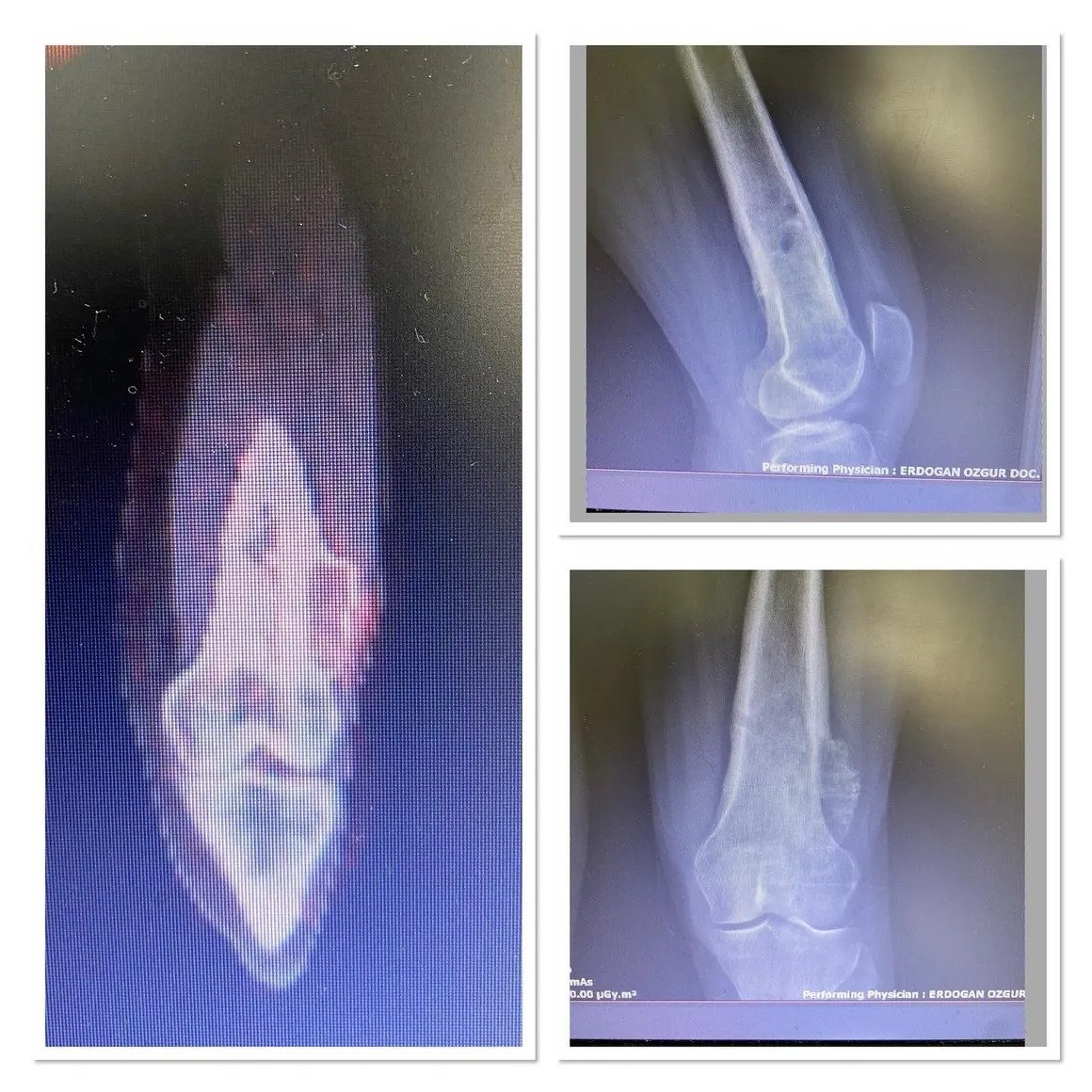
Диагностика начинается с подробного сбора анамнеза жалоб пациента, детального осмотра и классической рентгенографии. Доброкачественные опухоли обычно рассматриваются как образования, не вызывающие никаких жалоб, имеющие географические особенности, склеротические края и не вызывающие деструкцию костей или периостальную реакцию.
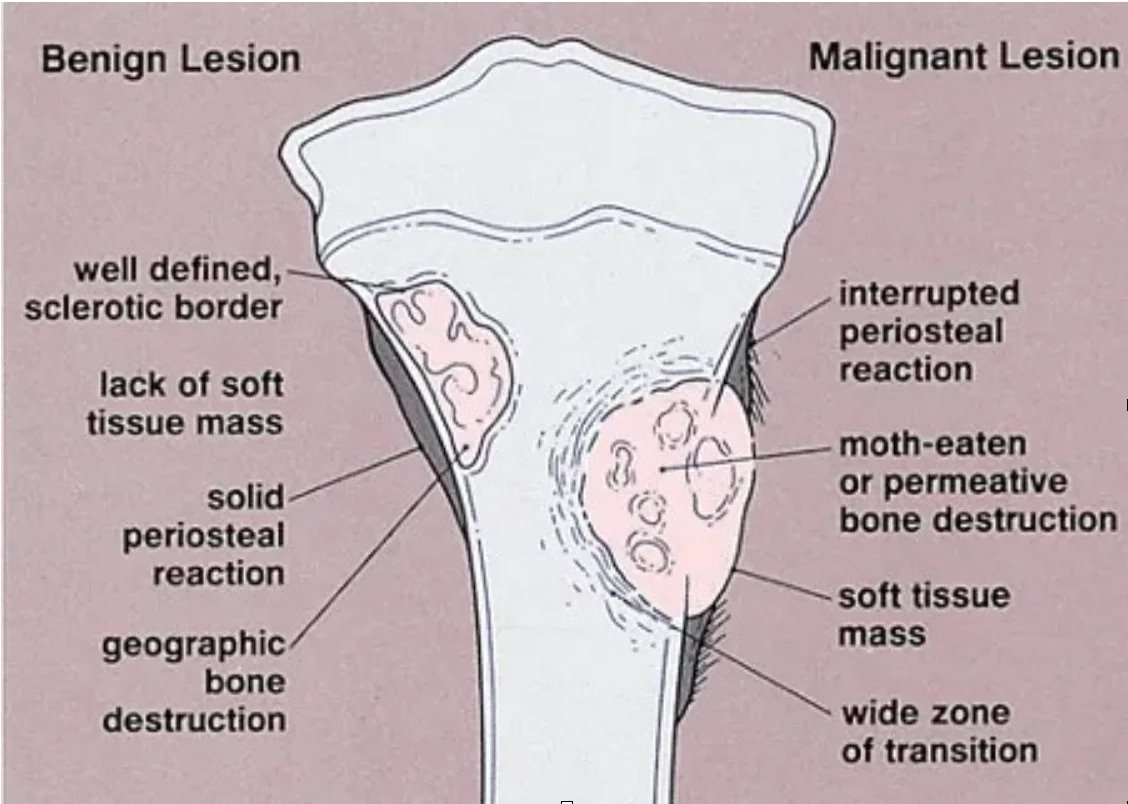
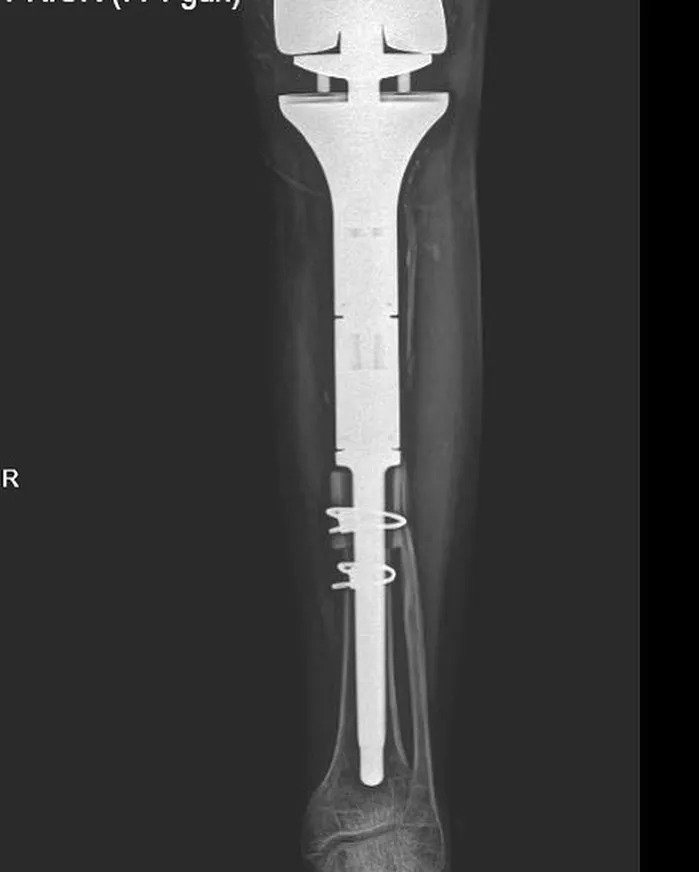
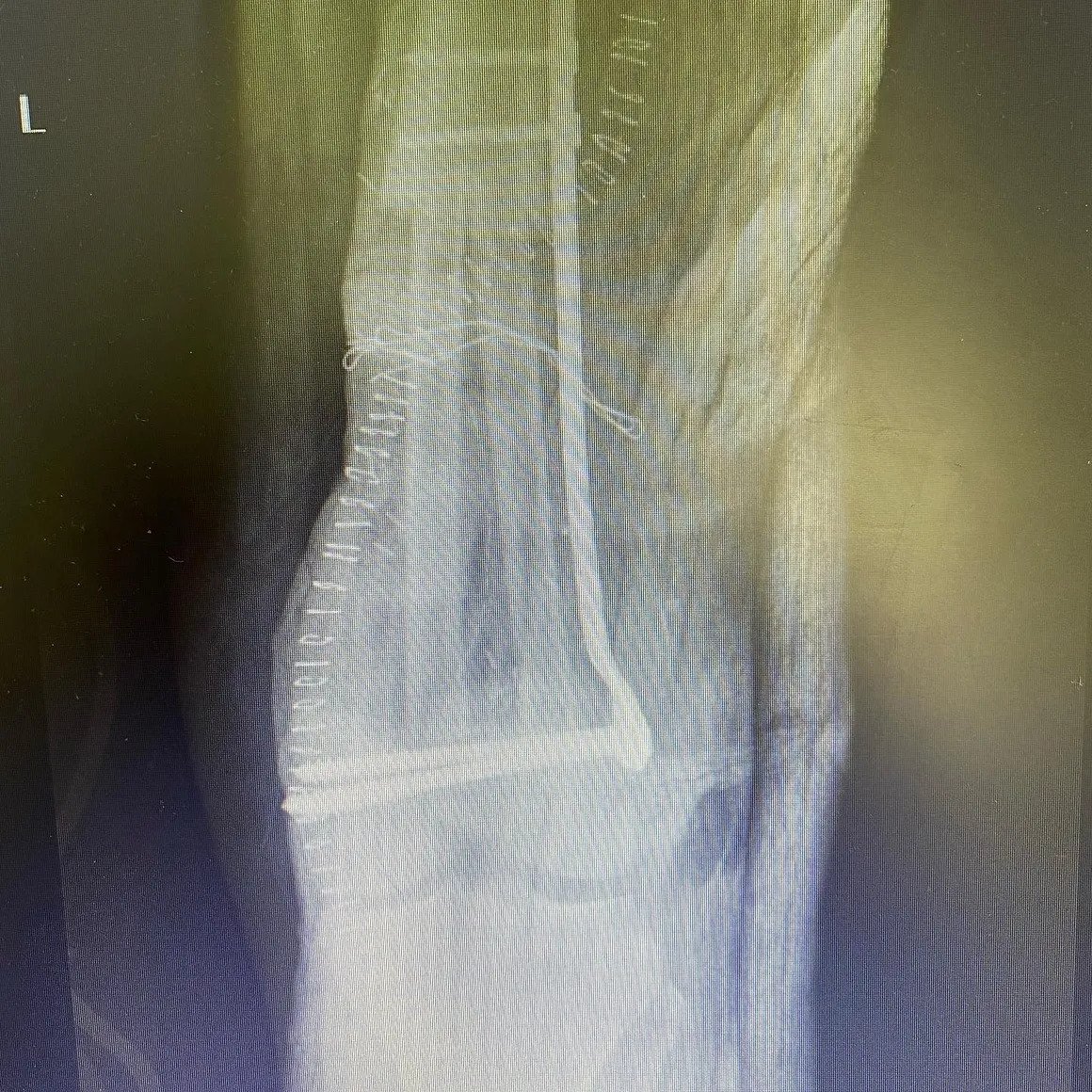
Злокачественные опухоли, с другой стороны, вызывают региональную боль и показывают литический, проникающий рост и нечеткие границы с неповрежденной костью на рентгенограммах. Могут наблюдаться разрушение костной оболочки и/или периостальная реакция (рисунок 2).
На этом этапе классический ортопед должен направить своего пациента к специалисту по опухолям-ортопеду. Расширенная визуализация и биопсия — это методы, которые должен определить ваш онколог.
Клиника опухолей костей
Клиника очень разнообразна. Поражения у пациентов могут возникать случайно или с такими симптомами, как боль и отек. Например, фиброзная дисплазия или остеохондроматоз могут возникать с искривлением костей у пациентов. Переломы, мягкотканные массы и отек могут возникать вместе с опухолью в кости. Болезненные поражения обычно наблюдаются при агрессивных (доброкачественных, но агрессивных) и потенциально злокачественных опухолях. Поскольку клинический спектр доброкачественных и злокачественных опухолей очень широк, диагностику должен проводить врач, имеющий опыт в хирургии опухолей. Неправильные и неадекватные диагнозы и методы лечения подвергнут пациента, которого можно было бы вылечить с помощью простого последующего наблюдения или лечения, ненужным, дорогим и вредным тестам и методам лечения. Аналогично, неадекватная диагностика и лечение агрессивных и злокачественных опухолей может привести к потере конечностей или смерти.
Клиника доброкачественных опухолей
Может быть умеренная боль, которая снимается обезболивающими. Боль возникает медленно и может быть связана с активностью или травмой. Например, ночная боль, которая реагирует на обезболивающие, типична для остеоидной остеомы. Переломы, которые возникают при движении, которое обычно не ломает кость, называются патологическими переломами. В некоторых доброкачественных поражениях патологические переломы могут развиваться при однократных или повторных травмах. ЕСЛИ ПОРАЖЕНИЕ ОБНАРУЖЕНО СЛУЧАЙНО, ПОКА У ПАЦИЕНТА НЕТ БОЛИ ИЛИ СИМПТОМОВ, ТО ОНИ, САМОЙ ВЕРОЯТНОЙ, ПОЛЕЗНЫ.
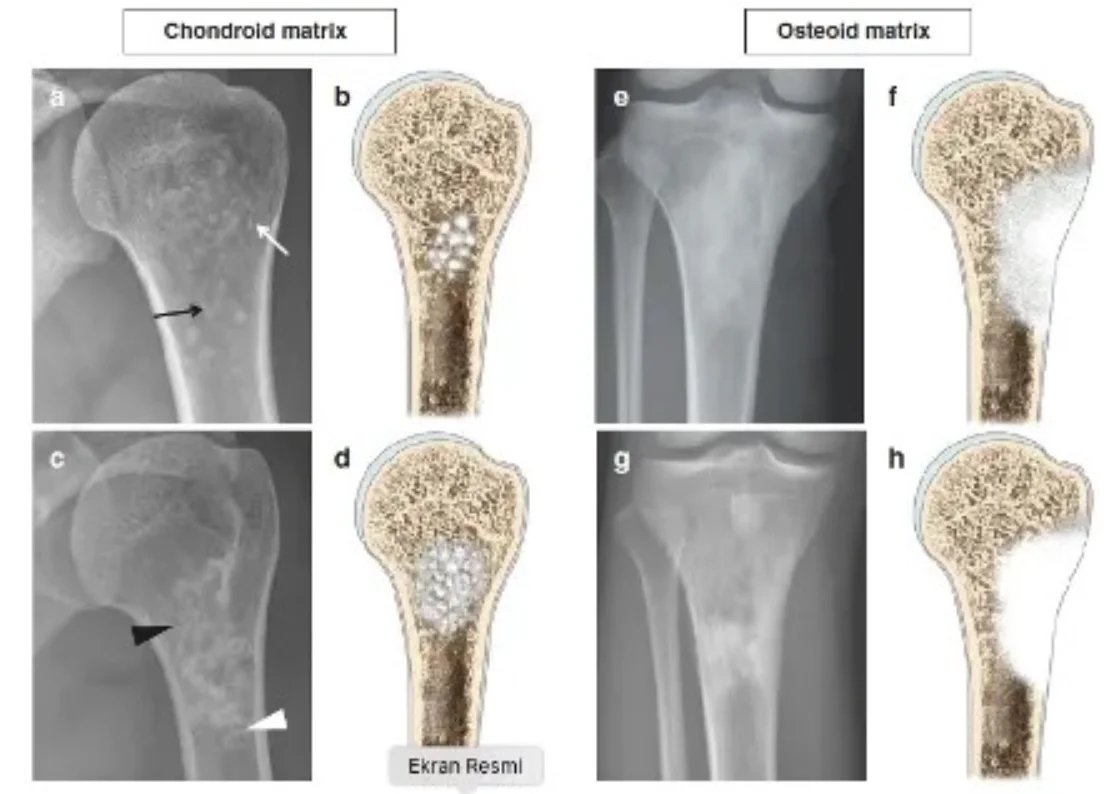
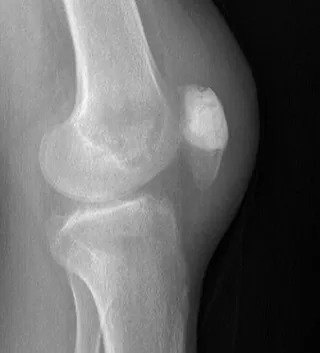
Опытный хирург-онколог поймет, является ли поражение хорошим или требует биопсии, на основе возраста пациента, расположения поражения и рентгенограммы. Рентгенологическое исследование должно охватывать всю кость. Доброкачественные опухоли, как правило, географические, имеют узкие переходные зоны и склеротические края (рисунок 1). Может наблюдаться истончение эндоста, но разрушение коркового слоя встречается редко. Другим полезным критерием диагностики является матрица поражения.
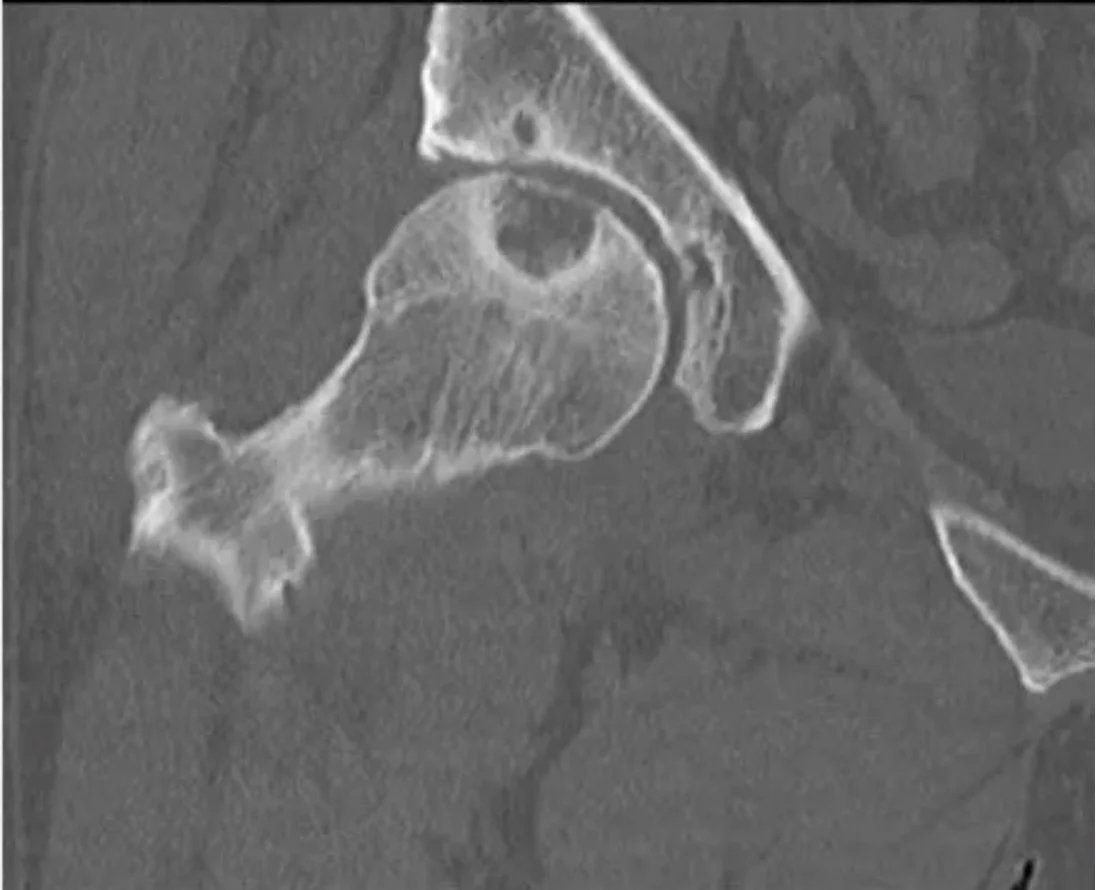
МРТ показывает компонент мягких тканей, задержку контрастного вещества, отек костного мозга и сигнальные характеристики поражения. Сцинтиграфия эффективна при полиостатической фиброзной дисплазии, множественном энхондроматозе и гистиоцитозе для выявления множественных поражений костей. Холодная сцинтиграфия не указывает на то, что поражение является агрессивным или незлокачественным (например, множественная миелома, метастазы почечно-клеточного рака). Дегенеративные и чрезмерно используемые поражения в поражениях, прилегающих к суставу, также включаются в дифференциальную диагностику.
Если есть разрушение коркового вещества, проникающий рост и периостальная реакция, необходимо дальнейшее обследование. Если диагноз не ясен, несмотря на КТ и МРТ, требуется биопсия. После постановки диагноза доброкачественной опухоли кости наблюдение и последующее наблюдение могут проводиться с интервалом в 3-6 месяцев для обеспечения радиологической стабильности. Хирургическое вмешательство потребуется для остановки разрушения кости, обнаружения патологических переломов или укрепления поражений, которые вот-вот сломаются, и предотвращения деформаций.
Клиника злокачественных опухолей
Клиника очень разнообразна. Поражения у пациентов могут возникать случайно или с такими симптомами, как боль и отек. Например, у пациентов с фиброзной дисплазией или остеохондроматозом обычно наблюдаются признаки искривления костей. Боль часто бывает сильной, и обезболивающие неэффективны. Боль тупая и глубокая, не связанная с активностью или покоем. Если происходит патологический перелом, боль возникает внезапно. Онемение в стопах и ногах, слабость, дисфункция кишечника и мочевого пузыря наблюдаются при опухолях позвоночника и крестца. Может быть сопутствующий отек. Могут наблюдаться утомляемость, слабость и лихорадка. В лабораторных условиях можно обнаружить повышенную щелочную фосфатазу, повышенный кальций и анемию. В анамнезе важен семейный анамнез рака и саркомы. Например, ретинобластома, синдром Ли Фраумени и синдромы Ротмунда-Томпсона оказывают предрасполагающее действие на опухоли костей, такие как остеосаркома. Сообщалось, что множественные поражения энхондроматозом могут ухудшаться. Кроме того, саркома может развиться у пациентов с болезнью Педжета, с историей лучевой терапии, хроническим остеомиелитом и инфарктом кости. Биопсию должен проводить хирург-ортопед, поскольку биопсия должна быть максимально закрытой, а это требует опыта. Кроме того, место биопсии должно быть выбрано таким образом, чтобы не загрязнять важные сосуды и нервы. Место биопсии должно находиться на линии, которую предпочитает хирург, проводящий операцию по удалению опухоли, при фактической операции по удалению опухоли. В противном случае потребуются длительные и тяжелые операции, такие как серьезные потери мышц и тканей, опасные сосудистые трансплантации, потери нервов и пересадки кожи. Это может увеличить потерю конечностей и сократить продолжительность жизни. Если диагностирована злокачественная опухоль кости, следует провести стадирование. Для этого необходимо быстро провести ПЭТ-визуализацию. У пациентов старше 40 лет поражение обычно представляет собой метастатическую карциному, множественную миелому или лимфому. Кроме того, следует оценить молочную железу у женщин и простату у мужчин и провести электрофорез белков в сыворотке и моче. Лечение может потребовать междисциплинарного подхода, включая лучевую терапию и онкологов-медиков под руководством ортопеда-онколога. Переломы, мягкие ткани и отеки могут возникать вместе с опухолью в кости. Болезненные поражения обычно наблюдаются при агрессивных (доброкачественных, но агрессивных) и потенциально злокачественных опухолях. Поскольку клинический спектр доброкачественных и злокачественных опухолей очень широк, диагностику должен проводить врач, имеющий опыт в хирургии опухолей. Неправильные и неадекватные диагнозы и методы лечения подвергают пациента, которого можно было бы вылечить с помощью простого последующего наблюдения или лечения, ненужным, дорогим и разрушительным тестам и методам лечения. Аналогично, неадекватная диагностика и лечение агрессивных и злокачественных опухолей могут привести к потере конечностей или смерти.
Опухоли мягких тканей
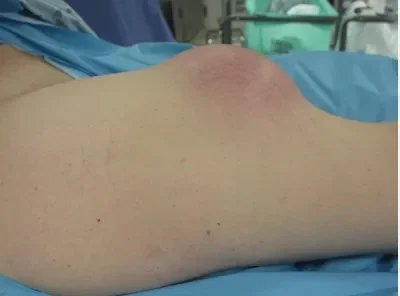
Опухоли мягких тканей встречаются чаще, чем опухоли костей, и часто являются доброкачественными. Процесс диагностики начинается с подробного анамнеза и обследования. Рентген, МРТ, УЗИ, КТ и ПЭТ используются для расширенного обследования. Эти инструменты также используются для оценки ответа на лечение. Доброкачественные опухоли встречаются в 100 раз чаще злокачественных. Расположение, размер и консистенция массы важны при сборе анамнеза и обследовании. Ее глубина проверяется относительно фасции.
Вопросы, которые следует задать:
- Когда было замечено образование?
- Есть ли увеличение в размерах?
- Какова скорость роста?
- Есть ли уменьшение в размерах?
- Есть ли сопутствующее образование?
- Есть ли боль, покраснение кожи, отек регионарных лимфатических узлов?
- Есть ли лихорадка, озноб, ночная потливость?
Кроме того, следует задать вопросы о таких проблемах, как травмы, прием антикоагулянтов, перенесенный рак и путешествия по миру.
НЕБОЛЬШАЯ, МЯГКАЯ, ПОВЕРХНОСТНАЯ И СТАБИЛЬНАЯ МАССА В ТЕЧЕНИЕ ЛЕТ, ВЕРОЯТНО, ПОЛЕЗНА.
БОЛЬШИЕ, ТВЕРДЫЕ, ГЛУБОКИЕ И РАСТУЩИЕ МАССЫ ИМЕЮТ ВЫСОКУЮ ВЕРОЯТНОСТЬ БЫТЬ ЗЛОКАЧЕСТВЕННЫМИ.
Гематомы могут возникнуть при легкой травме у людей, принимающих антикоагулянты, но эти гематомы могут скрывать лежащий в основе рак.
Наличие окостенения в массе помогает в дифференциальной диагностике. Например, в доброкачественной массе из-за травмы, называемой миозитом оссифицирующим, окостенение происходит на периферии (периферическое), в то время как в остеосаркоме мягких тканей (злокачественной) оно происходит в центре. Кальцификация имеет более дезорганизованный вид, чем окостенение. Флеболиты можно увидеть в сосудистых мальформациях, а дистрофические кальцификации можно увидеть в некоторых липомах. Если эта дистрофическая кальцификация кажется агрессивной, диагноз предполагает синовиальную саркому, которая является чрезвычайно злокачественной. Если вокруг сустава есть множественные однородные кальцификации, следует подумать о доброкачественной опухоли, называемой синовиальным хондроматозом. Агрессивная периостальная реакция или кортикальная деструкция, наблюдаемая в окружающей костной ткани, прилегающей к массе на рентгенограмме, должны предполагать высокую вероятность того, что масса плохая. Высокий сигнал на Т2 при МРТ, образование размером более 3 см, находящееся под фасцией, периферический отек, кровоизлияние в образовании, неоднородность на Т1, некроз опухоли, инвазия кости или сосудистого нерва, периферическое, узловое, неоднородное контрастное усиление указывают на то, что образование, скорее всего, плохое.
Благодаря использованию медикаментов в МРТ (контрастная МРТ) определяются гематомы, кистозно-солидное различие, кистозно-некротические области внутри массы, и таким образом выделяется наиболее подходящее место биопсии. Однако как кистозные массы, так и опухоли, богатые миксоидной структурой, могут светиться на жидкостно-чувствительных последовательностях. Эти массы можно различить только с помощью медикаментозной МРТ. В кистозных массах лекарство удерживает лекарство на периферии, в то время как солидные массы удерживают твердый контраст.
Если до операции была назначена радиотерапия и/или химиотерапия, необходимо исследовать опухоль с помощью новой МРТ перед операцией. Таким образом, можно понять реакцию на лечение. Иногда, несмотря на эти методы лечения, масса может расти, одной из причин этого является то, что масса начинает отмирать и кровоточить изнутри, что можно выявить с помощью медикаментозной МРТ.
Саркомы
Саркома — злокачественная опухоль, тип рака, возникающий из трансформированных клеток мезенхимального (соединительнотканного) происхождения. Соединительная ткань — это широкий термин, который включает костную, хрящевую, жировую, сосудистую или кроветворную ткани, и саркомы могут возникать в любом из этих типов тканей. В результате существует множество подтипов саркомы, классифицируемых в соответствии с конкретной тканью и типом клеток, из которых возникла опухоль. Саркомы — это первичные опухоли соединительной ткани, то есть они возникают из соединительной ткани.
Это контрастирует со вторичными (или «метастатическими») опухолями соединительной ткани, которые возникают, когда рак из другой части тела (например, легких, молочной железы или простаты) распространяется на соединительную ткань. Слово саркома происходит от греческого слова σάρκωμα sarōma «мясистый стул или вещество», которое в свою очередь происходит от σάρξ sarx, что означает «плоть».
Классификация
Саркомы обычно делятся на две основные группы: саркомы костей и саркомы мягких тканей, каждая из которых имеет несколько подтипов[2]. В Соединенных Штатах Американский объединенный комитет по борьбе с раком (AJCC) публикует руководства, классифицирующие подтипы саркомы.
Эти подтипы следующие:
Подтипы костной саркомы:
- Остеосаркомахондросаркома
- Низкодифференцированные круглоклеточные/веретеноклеточные опухоли (включая саркому Юинга) гемангиоэндотелиома
- ангиосаркома
- Фибросаркома/миофибросаркомахордома
- Адамантима
Другие:
- Липосаркомалейомиосаркома
- Злокачественная опухоль оболочки периферического нерва
- Рабдомиосаркома
- Синовиальная саркома
- Злокачественная солитарная фиброзная опухоль
Подтипы саркомы мягких тканей:
- Липосаркома (включает следующие типы: атипичная липоматозная опухоль/высокодифференцированная липосаркома, дедифференцированная липосаркома, миксоидная липосаркома, плеоморфная липосаркома и миксоидная плеоморфная липосаркома
- Дерматофибросаркома выбухающая (включает пигментированные разновидности)
- Дерматофибросаркома выбухающая, фибросаркоматоз
- Гигантоклеточная фибробластома
- Злокачественная солитарная фиброзная опухоль
- Воспалительная миофибробластическая опухоль
- Низкодифференцированная миофибробластическая саркома
- Фибросаркома (включает взрослые и склерозирующие эпителиоидные разновидности)
- Миксофибросаркома (ранее миксоидная злокачественная фиброзная гистиоцитома)
- Фибромиксоидная саркома низкой степени злокачественности
- Гигантоклеточная опухоль мягких тканей (лейомиосаркома)
- Злокачественная опухоль гломуса
- Рабдомиосаркома (включает: эмбриональную, альвеолярную, плеоморфную и веретеноклеточную/склерозирующую)
- Гемангиоэндотелиома (включает: ретиформную, псевдомиогенную и эпителиоидную)
- Ангиосаркома мягких тканей
- Внескелетная остеосаркома
- Желудочно-кишечная стромальная опухоль, злокачественная (GIST)Злокачественная оболочка периферического нерва опухоль (включая эпителиоидную разновидность)
- Злокачественная опухоль Тритона
- Злокачественная опухоль зернистых клеток
- Злокачественная оссифицирующая фибромиксоидная опухоль
- Стромальная саркома, не указанная отдельно
- Миоэпителиальная карцинома
- Злокачественная фосфатурическая мезенхимальная опухоль
- Синовиальная саркома (включая: веретеноклеточную, двухфазную и не указанную отдельно)
- эпителиоидная саркома
- Альвеолярная мягкотканная саркома
- Светлоклеточная саркома мягких тканей
- Внескелетная миксоидная хондросаркомаВнескелетная
- Саркома ЮингаСаркома интердигитирующих дендритных клеток
- Десмопластическая мелкокруглоклеточная опухоль
- Экстраренальная рабдоидная опухоль
- Периваскулярная эпителиоидноклеточная опухоль, не указанная отдельно
- Интимальная саркома
- Недифференцированная веретеноклеточная саркома
- Недифференцированная плеоморфная саркома
- Недифференцированная круглоклеточная саркома
- Недифференцированная эпителиоидная саркома
- Недифференцированная саркома, не указанная отдельно.
Симптомы саркомы:
Симптомы сарком костей обычно включают боль в костях, особенно ночью, и отек вокруг места опухоли.
Симптомы сарком мягких тканей различаются, но обычно они представляют собой твердые, безболезненные уплотнения или узелки. Гастроинтестинальные стромальные опухоли (подтип саркомы мягких тканей) обычно бессимптомны, но могут быть связаны с неопределенными жалобами, такими как боль в животе, чувство переполнения или другие признаки кишечной непроходимости.
Причины и факторы риска:
Причина большинства сарком костей неизвестна, но несколько факторов связаны с повышенным риском развития саркомы костей. Предшествующее воздействие ионизирующего излучения (например, предыдущая лучевая терапия) является одним из таких факторов риска. Воздействие алкилирующих агентов, таких как те, которые содержатся в некоторых химиотерапевтических препаратах для лечения рака, также увеличивает риск развития саркомы костей. Некоторые наследственные генетические синдромы, включая синдром Ли-Фраумени, наследственные мутации гена RB1 и болезнь Педжета, связаны с повышенным риском развития сарком костей.
Большинство сарком мягких тканей вызваны тем, что врачи называют «спорадическими» (или случайными) генетическими мутациями в клетках пораженного человека. Однако существуют определенные факторы риска, связанные с повышенным риском развития саркомы мягких тканей. Предшествующее воздействие ионизирующего излучения является одним из таких факторов риска. Воздействие винилхлорида (например, паров, встречающихся при производстве поливинилхлорида (ПВХ)), мышьяка и торотраста связано с повышенным риском развития ангиосаркомы. Лимфедема, например, возникающая в результате некоторых видов лечения рака молочной железы, также является фактором риска развития ангиосаркомы. Как и в случае с костными саркомами, некоторые наследственные генетические синдромы, включая синдром Ли-Фраумени, семейный аденоматозный полипоз, нейрофиброматоз типа 1 и наследственные мутации гена RB1, также связаны с повышенным риском развития сарком мягких тканей. Саркома Капоши вызывается вирусом герпеса, ассоциированным с саркомой Капоши (HHV-8).
Механизмы:
Хотя точные молекулярные изменения, которые приводят к саркоме, не всегда известны, некоторые типы саркомы связаны с определенными генетическими мутациями.
Примеры включают:
Большинство случаев саркомы Юинга связаны с хромосомной транслокацией, при которой часть хромосомы 11 присоединяется к части хромосомы 22.[2] Это приводит к слиянию гена EWS с другими генами, включая ген FLI1 в 90% случаев Юинга и ген ERG в 5-10% случаев. Эти слияния вызывают выработку аномальных белков, но точно неизвестно, как эти аномальные белки вызывают рак.
Выбухающая дерматофибросаркома часто связана с хромосомной транслокацией, при которой ген COL1A1 сливается с геном PDGFRB. Это приводит к сверхактивной сигнализации PDGF, которая, как полагают, способствует делению клеток и в конечном итоге приводит к развитию опухоли.
Воспалительная миофибробластическая опухоль часто связана с перестройками гена ALK и иногда с перестройками гена HMGA2.
Гигантоклеточная опухоль мягких тканей часто связана с хромосомной транслокацией между хромосомой 1 и хромосомой 2, где ген CSF1 сливается с геном COL6A3. Это вызывает повышенную выработку белка CSF1, который, как полагают, играет роль в развитии рака.
Многие липосаркомы связаны с дупликацией части хромосомы 12, что приводит к появлению дополнительных копий известных генов, способствующих развитию рака («онкогенов»), таких как ген CDK4, ген MDM2 и ген HMGA2.
Диагностика:
Саркомы костей
Диагностика сарком костей начинается с подробного анамнеза и физического обследования, которые могут выявить характерные признаки и симптомы (см. Признаки и симптомы выше). Хотя некоторые саркомы костей (например, остеосаркома) могут быть связаны с повышенным уровнем щелочной фосфатазы, а другие (например, саркома Юинга) с повышенной скоростью оседания эритроцитов, лабораторные исследования не особенно полезны для диагностики. Однако важно то, что ни один из этих лабораторных результатов не является специфичным для сарком костей; это означает, что повышение этих лабораторных показателей связано со многими другими состояниями, помимо саркомы, и поэтому на них нельзя полагаться для окончательной диагностики саркомы. Визуальные исследования имеют решающее значение для диагностики, и большинство врачей изначально назначают простую рентгенограмму (рентген). Другие визуальные исследования, обычно используемые в диагностике, включают исследования магнитно-резонансной томографии (МРТ) и радиоизотопное сканирование костей. Хотя компьютерная томография (КТ) является важным инструментом для стадирования, она обычно не используется для диагностики большинства типов сарком костей. Окончательный диагноз требует биопсии опухоли и тщательного изучения образца биопсии опытным патологом.
Саркомы мягких тканей
Диагностика сарком мягких тканей начинается с подробного анамнеза и физического обследования. Исследования с помощью визуализации могут включать КТ или МРТ, но КТ, как правило, предпочтительнее для сарком мягких тканей, расположенных в грудной клетке, брюшной полости или забрюшинном пространстве. Позитронно-эмиссионная томография (ПЭТ) также может быть полезна для диагностики, но чаще всего ее используют для стадирования. Как и в случае с саркомами костей, окончательный диагноз требует биопсии и оценки гистологии обученным патологом.
Стадирование:
В целом, стадирование рака относится к тому, насколько запущен рак, и часто основывается на таких факторах, как размер опухоли и ее распространение на другие части тела. Стадирование важно, поскольку стадия влияет на прогноз (вероятный результат), а также на типы лечения, которые, вероятно, будут эффективны против рака. При стадировании сарком проверяется, проросла ли опухоль в окружающие ткани (местное проникновение), распространилась ли на лимфатические узлы (лимфатические метастазы) или проникла в другие ткани или органы тела (отдаленные метастазы).
Наиболее распространенными инструментами визуализации, используемыми для стадирования костных сарком, являются МРТ или КТ для оценки первичной опухоли, КТ грудной клетки с контрастным усилением для оценки того, распространился ли рак (т. е. метастазировал) на легкие, и радиоизотопное сканирование костей для оценки метастазов в кости. Стадирование сарком мягких тканей обычно включает визуализацию первичной опухоли с помощью МРТ или КТ для определения размера опухоли, а также КТ грудной клетки с контрастным усилением для оценки метастатических опухолей в легких.
Степень:
Как и некоторым другим видам рака, саркомам присваивается степень (низкая, средняя или высокая) на основе внешнего вида опухолевых клеток под микроскопом. В целом степень относится к тому, насколько агрессивен рак и насколько вероятно его распространение («метастазирование») в другие части тела. Саркомы низкой степени имеют лучший прогноз, чем саркомы высокой степени, и обычно лечатся хирургическим путем. Саркомы средней и высокой степени чаще лечатся с помощью комбинации хирургии, химиотерапии или лучевой терапии. Поскольку опухоли высокой степени чаще метастазируют (проникают и распространяются в региональные и отдаленные органы), их лечат более агрессивно. Знание того, что многие саркомы чувствительны к химиотерапии, значительно улучшило выживаемость пациентов. Например, в эпоху до химиотерапии долгосрочная выживаемость у детей с локализованной остеосаркомой составляла всего 20%, но сейчас она возросла до 60–70%.
Лечение
Наиболее распространенным методом лечения большинства сарком, которые не распространились на другие части тела, является хирургическое вмешательство. Теперь мы проводим органосохраняющие операции, а не ампутацию, чтобы спасти конечности пациентов по крайней мере в 90% случаев саркомы конечностей (руки или ноги). Дополнительные методы лечения, включая химиотерапию, лучевую терапию (также называемую «радиотерапией») и протонную терапию, могут назначаться до операции (так называемая «неоадъювантная» химиотерапия или радиотерапия) или после операции (так называемая «адъювантная» химиотерапия или радиотерапия). Использование неоадъювантной или адъювантной химиотерапии и радиотерапии значительно улучшило прогноз для многих пациентов с саркомой. Лечение может быть длительным и трудным процессом, занимающим около года для многих пациентов.
Прогноз
Факторы, влияющие на прогноз
AJCC определил несколько факторов, которые влияют на прогноз сарком костей:
Размер опухоли:Более крупные опухоли, как правило, имеют худший прогноз, чем меньшие опухоли.
Распространение опухоли на окружающие ткани: Опухоли, которые локально распространились на окружающие ткани, как правило, имеют худший прогноз, чем опухоли, которые не распространились за пределы места своего возникновения.
Стадия и наличие метастазов: Опухоли, которые распространились («метастазировали») в лимфатические узлы (редко для сарком костей) или другие органы или ткани (например, легкие), имеют худший прогноз, чем опухоли, которые не распространились.
Степень злокачественности опухоли:опухоли высокой степени злокачественности (степени злокачественности 2 и 3), как правило, имеют худший прогноз, чем опухоли низкой степени злокачественности (степени злокачественности 1).
Расположение в скелете:Опухоли, возникающие из позвоночника или костей таза, как правило, имеют худший прогноз, чем опухоли, возникающие из костей рук или ног.
Факторы, влияющие на прогноз для сарком мягких тканей, отличных от GIST, включают:
Степень злокачественности: AJCC рекомендует использовать систему градации, называемую группой сарком Французской федерации онкологических центров (FNCLCC) для сарком мягких тканей, где опухоли высокой степени злокачественности имеют худший прогноз, чем опухоли низкой степени злокачественности. p>
Key factor affecting prognosis for GISTs:
Mitotic rate: mitotic rate refers to the fraction of cells actively dividing within the tumor; GISTs with a high mitotic rate have a worse prognosis than GISTs with a low mitotic rate.
Данные результатов
Согласно данным, опубликованным Национальным институтом рака США (NCI), общая 5-летняя выживаемость при саркомах костей составляет 66,9%. Американское онкологическое общество (ACS) оценивает, что в 2019 году в США от сарком костей умрут 1660 человек, что составит 0,3% всех случаев смерти от рака. Средний возраст смерти составляет 61 год, но смерть может наступить в любой возрастной группе. Таким образом, 12,3% случаев смерти от саркомы костей приходится на людей в возрасте до 20 лет, 13,8% — на людей в возрасте от 20 до 34 лет, 5,5% — на людей в возрасте от 35 до 44 лет и 9,3% — на людей в возрасте от 45 до 54 лет. 13,5% у людей в возрасте 55-64 лет, 16,2% у людей в возрасте 65-74 лет, 16,4% у людей в возрасте 75-84 лет и 13,1% у людей в возрасте 85 лет и старше. Наблюдается у людей старше.
Общая 5-летняя выживаемость при саркомах мягких тканей (независимо от стадии) составляет 64,5%, но на выживаемость влияют многие факторы, включая стадию. Таким образом, 5-летняя выживаемость составляет 80,8% для сарком мягких тканей, которые не распространились за пределы первичной опухоли («локализованные» опухоли), 58,0% для сарком мягких тканей, которые распространились только на близлежащие лимфатические узлы, и 16% для сарком мягких тканей с отдаленным распространением на органы. составляет .4. По оценкам ACS, в 2019 году от саркомы мягких тканей умрет 5270 человек, что составит 0,9% всех случаев смерти от рака.
Эпидемиология
Саркомы встречаются крайне редко. Риск того, что ранее здоровому человеку будет поставлен диагноз нового рака кости, составляет менее 0,001% (1 из 100 000), в то время как риск постановки диагноза новой саркомы мягких тканей составляет от 0,0014 до 0,005%. Американское онкологическое общество оценивает, что в 2019 году в Соединенных Штатах будет 3500 новых случаев саркомы костей и 12 750 новых случаев саркомы мягких тканей. Учитывая, что предполагаемое общее число новых диагнозов рака (всех типов рака) составляет 1 762 450, это говорит о том, что саркомы костей составляют всего 0,2% всех новых диагнозов рака (что делает их 30-м по распространенности типом рака). Саркомы мягких тканей составили всего 0,7% всех новых диагнозов рака в Соединенных Штатах в 2019 году (что делает их 22-м по распространенности типом рака).
Саркомы поражают людей всех возрастов. Примерно 50% сарком костей и 20% сарком мягких тканей диагностируются у людей моложе 35 лет. Некоторые саркомы, такие как лейомиосаркома, хондросаркома и желудочно-кишечная стромальная опухоль (GIST), чаще встречаются у взрослых, чем у детей. Большинство сарком костей высокой степени злокачественности, включая саркому Юинга и остеосаркому, гораздо чаще встречаются у детей и молодых людей.
Лечение:
Лечение саркомы часто требует химиотерапии, особенно когда саркома распространилась или «метастазировала», но современные химиотерапевтические препараты связаны со значительной токсичностью и не полностью эффективны в уничтожении раковых клеток. Поэтому с 2019 года проводятся исследования по выявлению новых препаратов для лечения саркомы. Одной из возможностей является использование иммунотерапии рака (например, ингибиторов иммунных контрольных точек, таких как агенты анти-PD1, анти-PDL1 и анти-CTLA4) для лечения сарком. Это еще не устоявшийся метод лечения. Также изучаются другие стратегии, такие как таргетная терапия малыми молекулами, биологические агенты (например, малые интерферирующие молекулы РНК) и терапия, ориентированная на наночастицы.
Д-р Самир Растоги и др. показал долгосрочные ответы на иммунотерапию при нескольких саркомах (UPS и ASPS).
Исследования продолжают изучать специфические генетические и молекулярные факторы, которые вызывают развитие саркомы. Это может позволить разработать новые таргетные терапии и позволить врачам более точно предсказывать прогноз для пациента.
Наличие рецептора иммунорегуляторной контрольной точки H3-B3 на опухолевых клетках дает возможность для клинических испытаний новых препаратов и таргетных агентов, а также иммунотерапии в разработке.
Осведомленность:
В Соединенных Штатах июль широко признан месяцем осведомленности о саркоме. В Великобритании в июле проходит Неделя осведомленности о саркоме, проводимая благотворительной организацией по борьбе с раком костей и мягких тканей Sarcoma UK.
Американскому ютуберу Technoblade поставили диагноз саркома в августе 2021 года, и он умер от этой болезни в июне 2022 года после того, как рак дал метастазы. Он собрал более 500 000 долларов в благотворительной кампании. Многие ютуберы повышали осведомленность и делали пожертвования в благотворительные организации, такие как Sarcoma Foundation of America, после того, как Technoblade поставили диагноз и он скончался.
Биопсия
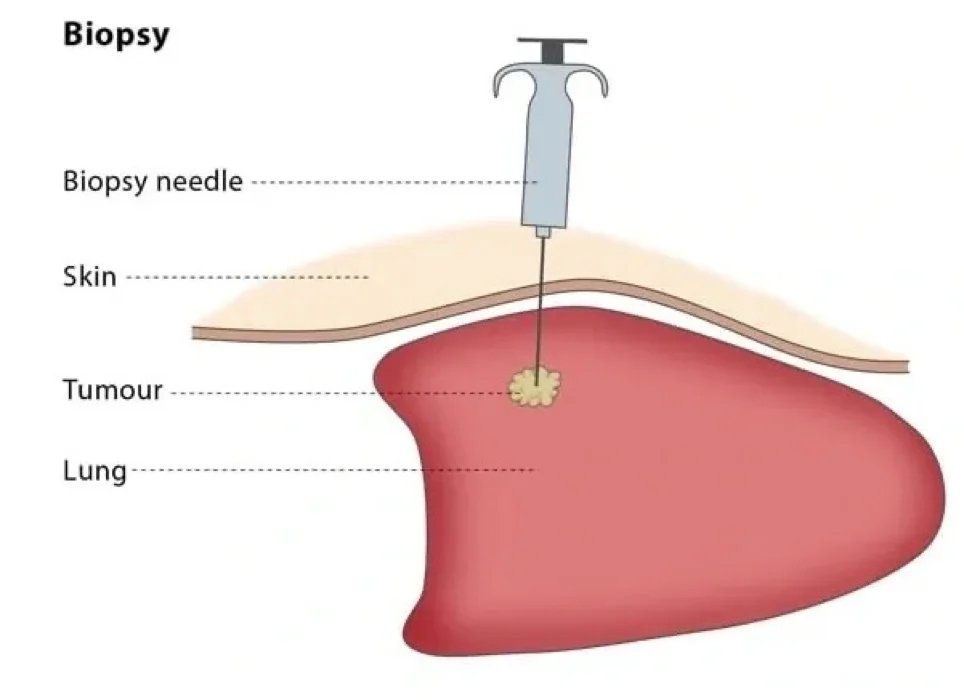
Одним из важнейших этапов диагностики и лечения опухолей опорно-двигательного аппарата является биопсия. Хорошо спланированная и выполненная биопсия сведет к минимуму травмы, которые могут возникнуть из-за болезни. Среди населения распространено мнение, что нож нельзя применять к опухоли. На самом деле, я думаю, что это правда. По этой причине мы редко проводим открытую биопсию.
В последние годы, когда мы оценивали небольшие образцы, взятые без вскрытия опухоли с помощью специальных игл с опытными инструкторами по патологии, мы начали ставить диагнозы с высокой точностью. Поскольку мы берем биопсию иглой и закрытым методом, распространение опухолевых клеток минимально. Основной принцип хирургии опухолей — удалить массу, не видя опухоль и не проникая в нее, оставляя немного здоровой ткани вокруг. Другими словами, опухоль не должна быть действительно проколота.
Принципы биопсии:
- Операцию по удалению рака нельзя проводить без постановки диагноза рака.
- Перед биопсией необходимо провести клиническую и рентгенологическую оценку.
- Хотя доброкачественные опухоли встречаются гораздо чаще злокачественных, всегда следует учитывать диагноз рака.
- В большинстве случаев достаточно закрытой биопсии, и она должна быть предпочтительнее.
- Если необходимо провести открытую биопсию, ее должен проводить хирург, который будет проводить операцию.
- Метод, называемый эксцизионной биопсией (рассматривающий всю опухоль как материал для биопсии, не захватывая никакой части и выполняя широкую резекцию), следует применять только в особых случаях.
- Диагностика и лечение саркомы — это командная работа. Необходимо доверить эту работу компетентным рукам.
Если следовать этим принципам, можно поставить наиболее точный диагноз с наименьшим вредом для пациента. Это:
- Липомы (жировые железы): если поражение однородно и изоинтенсивно с жировой тканью во всех последовательностях, биопсия не требуется
- Доброкачественные опухоли костей с типичной рентгенологией (остехондромы, неоссифицирующие фибромы, энхондромы, однокамерные простые костные кисты). Фактически, эти поражения могут не требовать дальнейшего обследования с помощью высококачественных рентгеновских лучей.
- В дополнение к липомам (мягкотканным массам с типичными результатами МРТ), шванномам, гемангиомам, артериовенозным мальформациям, миксомам.
- Метастазирующие поражения у пациентов с подтвержденной биопсией карциномой или миеломой
Обычно я провожу биопсию мягких тканей под местной анестезией в условиях офиса. Я провожу биопсию иглой примерно за десять минут, с минимальной болью. Пациент может вернуться на работу в тот же день. Несмотря на то, что я работаю с одним из наших самых опытных инструкторов по закрытой игольной биопсии, диагноз поставить удается редко. По этому вопросу некоторые авторы рекомендуют перейти на открытую биопсию, в то время как другие рекомендуют продолжать закрытую биопсию до тех пор, пока не будет поставлен диагноз. Лично я, если я дважды пробую закрытую биопсию и все равно не могу поставить диагноз, предпочитаю перейти на открытую биопсию.
Я провожу биопсию костей в операционной под скопической визуализацией, предпочтительно как закрытую игольную биопсию. Я беру образцы биопсии под общим наркозом в ходе процедуры, которая занимает около 15 минут, чтобы пациент не чувствовал никакой боли.
Если у пациента подозревают инфекцию во время визуализации, анализов крови или обследования перед процедурой, антибиотики следует прекратить, подождать не менее двух недель и провести посевы на аэробные, анаэробные, кислотоустойчивые бактерии и грибки. В прошлом подход, при котором культура должна быть взята из каждой биопсии, и биопсия должна быть взята из каждой культуры, был распространен. Однако благодаря современным методам визуализации и лабораторным методам стало возможным сузить вероятность заражения у пациентов, проходящих биопсию. Ненужные посевы могут привести к неправильной диагностике инфекции, что может подвергнуть пациента длительному, утомительному и дорогостоящему лечению антибиотиками.