EWİNG SARKOM TEDAVİSİ
Ewing sarkomu, çoğunlukla yaşamın ikinci on yılındaki ergenleri etkileyen ikinci en yaygın primer kötü huylu-malign kemik tümörüdür ve oldukça metastatik bir sarkom sınıfıdır. Radyoterapi veya cerrahi kullanımına rağmen, geçmişte hastaların tahminen %85 ila %90’ı metastaz nedeniyle birkaç ay içinde ölmüştür. Ama günümüzde hastalığın hem lokal terapi hem de çok ajanlı adjuvan kemoterapiyle tedavisindeki kayda değer ilerleme nedeniyle, 5 yıllık sağkalım oranı %20’nin altından %70’in üzerine çıktı. Ancak nüks oranı hala yüksek seyretmektedir. Yüksek morbidite ve mortaliteyi önlemek için derhal tanınmalı ve tedavi edilmelidir. Ewing sarkomu (ES), adolesan ve genç erişkinlerde görülen agresif bir tümör olup, tüm kemik sarkomlarının %10 ila %15’ini oluşturur.
James Ewing tarafından ilk kez 1921’de tanımlandı. Ewing sarkomu ailesinde ‘klasik’ kemik Ewing sarkomu, iskelet dışı Ewing sarkomu, göğüs duvarının kötü huylu küçük hücreli tümörü (Askin tümörü) ve yumuşak doku bazlı ilkel nöroektodermal tümörler (PNET) bulunmaktadır. t(11;22)(q24;q12) translokasyonu, tümörlerin %85’iyle ilişkilidir ve EWS-FLI-1 oluşumuna yol açarken, t(21;12)(22;12) ve diğer daha az yaygın translokasyonlar, EWS-FLI-1’i indükler. ERG füzyonu vakaların geri kalan %10 ila %15’ini oluşturur. En yaygın anatomik bölgeler arasında pelvis, aksiyal iskelet ve femur yer alır; ancak hemen hemen her kemik veya yumuşak dokuda ortaya çıkabilir. Tipik olarak hastalar tutulum bölgesinde ağrı ve şişlikle başvururlar. Çoğu lokal olarak mevcut olmasına rağmen, hemen hemen hepsinde subklinik metastatik hastalık mevcuttur. Başlangıçta lokalize hastalığı olan hastaların yaklaşık %25’i sonuçta nüksetmektedir.
Nükseden ve dirençli ES için standart bir tedavi mevcut değildir. ES ile çevresel risk faktörleri, ilaca maruz kalma, radyasyon öyküsü veya ailedeki kanser öyküsü arasında bir ilişki yoktur. Ewing sarkomu, çocukluk çağının küçük yuvarlak mavi hücreli tümörleri (örneğin, retinoblastoma, nöroblastom, rabdomiyosarkom ve nefroblastoma) ailesini temsil eden, artan nükleer sitoplazmik orana sahip küçük yuvarlak hücrelerden oluşur. Ewing hücrelerinde bol miktarda glikojen içeren yetersiz eozinofilik sitoplazma bulunur ve bu genellikle periyodik asit Schiff ile boyanarak tespit edilir. Vakaların %80’inden fazlasında yüksek CD99 ekspresyonu gösterilmiştir. Bu son derece hassas immünohistokimyasal biyobelirteç muhtemelen lökositlerin endotele sürekli göçünü kolaylaştırmada anahtar bir rol oynar; ancak diğer sarkom ve lenfomalarda da saptanabileceği için özgüllüğü yoktur. MIC2 gen ürünü CD99’a ek olarak Ewing hücreleri sıklıkla CD45, sinaptofizin, kromogranin, vimentin, vimentin, keratin, desmin, nörona özgü enolaz (NSE) ve S-100’ü eksprese eder. Ancak bu immünohistokimya paneli spesifiklik eksikliği nedeniyle sınırlandırılmıştır. Kesin ayrımı yapabilmek için floresan in situ hibridizasyon (FISH) ve/veya ters transkripsiyon-polimeraz zincir reaksiyonu (RT-PCR) kullanan moleküler genetik çalışmalara ihtiyaç vardır.
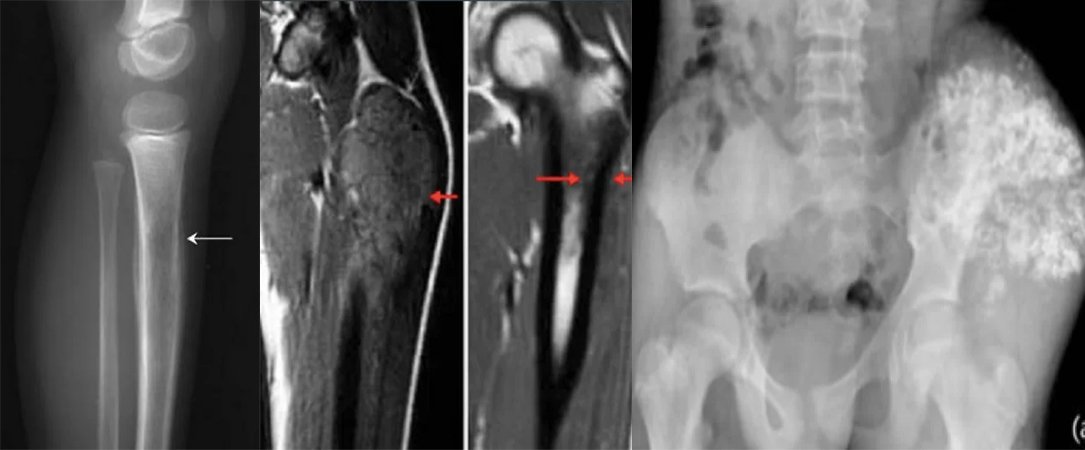
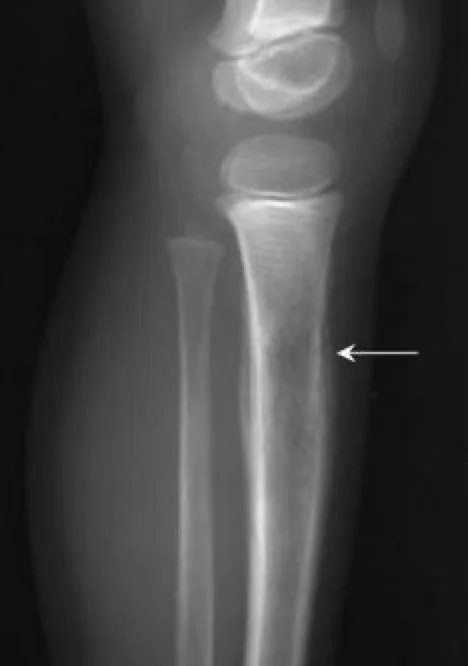
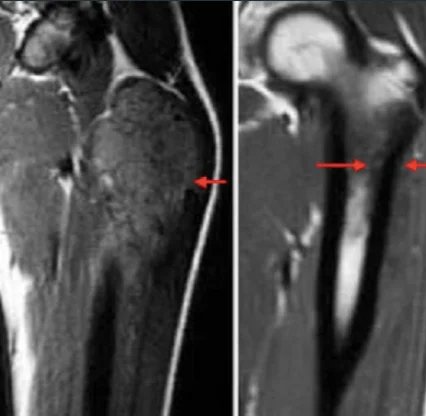
Ewing Sarkomu Bulgular: Ewing sarkomu olan hastalar genellikle birkaç hafta veya ay boyunca ağrı, sertlik veya şişlik gibi lokal semptomlarla başvururlar. ES’li hastaların %50’sinden fazlasında geceleri kötüleşen aralıklı ağrı vardır. Ewing sarkomu, farklı sunumlarla çok çeşitli yerlerde ortaya çıkabilir. Genellikle uzun kemiklerin diyafizinde bulunur. Uzun kemikteki kemik lezyonları veya metastatik lezyonlar patolojik kırıklar olarak ortaya çıkabilir. ES’nin pelvik konumu sırt ağrısı olarak ortaya çıkabilir. Ateş ve kilo kaybı gibi sistemik semptomların varlığı sıklıkla metastatik hastalığa işaret eder. Hastaların yaklaşık %20’si tanı anında metastatik hastalıkla başvurur ve bu olguların %20’sinden fazlasında akciğer veya plevra tutulumu vardır.
Kapsamlı bir fizik muayene önemlidir. Akciğer ve plevra metastazı durumunda hasta asimetrik nefes sesleri, plevral belirtiler veya raller ile başvurabilir. Kemik iliği metastazı olan hastalarda trombositopeniye bağlı peteşi veya purpura görülebilir. MSS tutulumu olan hastalarda nörolojik muayene de önemlidir. İlk incelemeler, etkilenen bölgenin röntgenini içerir; röntgende periosteal reaksiyonun “soğan zarı” görünümünü gösterebilir. Primer bölge ve potansiyel metastatik alanlar görüntüleme testleriyle değerlendirilmelidir. Etkilenen bölgenin düz radyografileri, kemikte yıkım oluşturan “güve yeniği” lezyonları, “Codman üçgeni” veya çok katmanlı “soğan zarı” periost reaksiyonunu gösterebilir. Güncellenmiş 2017 Ulusal Kapsamlı Kanser Ağı (NCCN) kılavuzuna göre, birincil bölgelerin görüntülenmesi Emar ve gereğinte BT ile yapılır ve Emarın kontrast madde verilerek çekilmesi birincil öneme sahiptir. Diğer görüntüleme yöntemleri arasında toraks BT, pozitron emisyon tomografisi (PET)/BT ve omurga/pelvis MRG’si yer alır. Semptomatik hasta, biyopsi gerekiyorsa ortopedik tümör cerrahına yönlendirilmelidir. Tanı tercihen iğne biyopsisi yada açık biyopsi ile konur. T(11;22) translokasyonunu değerlendirmek için biyopsi örneklerinin moleküler sitogenetik analizi tanı çalışmasına dahil edilmelidir. Kemik iliği aspirasyonu ve kemik iliği biyopsisi düşünülebilir. NCCN kurallarına göre, Prognostik önem taşıdığı için ilk değerlendirme serum laktat dehidrojenazı (LDH) içermelidir. Tedaviye başlama dan önce hastalara doğurganlık danışmanlığı (sperm yumurta dondurma) da sunulmalıdır.
Ewing Sarkomu Kemoterapi Ve Radyoterapi: Tarihsel olarak, Gruplararası Ewing Sarkom çalışmaları (IESS-I ve IESS-II), VAC (vinkristin, daktinomisin ve siklofosfamid) ile karşılaştırıldığında RT+VACA (vinkristin, daktinomisin, siklofosfamid ve doksorubisin) ile daha iyi sonuçlar göstermiştir. Daktinomisin rejimlerinde doksorubisin dozunun sınırlandırılması nedeniyle, daha sonra yapılan araştırmalar, daktinomisin hariç tutulduğunda klinik sonuçlar üzerinde anlamlı bir etki göstermedi. Birçok çalışma, standart kemoterapiye ifosfamid ve etoposidin eklenmesini değerlendirdi. Pediatrik Onkoloji Grubu-Çocuk Kanseri Grubu çalışması INT0091, VACD-IE grubunun VACD grubuna göre önemli ölçüde daha iyi hayatta kalma oranlarına sahip olduğunu gösterdi.
Ayrıca VACD-IE grubunda lokal başarısızlık insidansı daha düşüktü. EICESS-92 çalışmasında (Avrupa Gruplararası Kooperatif Ewing Sarkom Çalışması), standart riskli hastalarda (SR) VACA (vinkristin, daktinomisin, siklofosfamid ve doksorubisin) ve VAIA (vinkristin, daktinomisin, ifosfamid ve doksorubisin) karşılaştırıldı ve siklofosfamidin etkisinin ifosfamide benzer olduğu saptanmış; ancak siklofosfamid artan toksisiteyle ilişkilendirilmiştir. 3 yıllık olaysız sağkalım (EFS) oranları VACA ve VAIA için sırasıyla %73 ve %74 idi. Euro-EWING99-R1 çalışması (EICESS-92 protokolüne dayanan eşdeğerlik çalışması), standart riskli hastalarda vinkristin ve daktinomisin dahil konsolidasyon tedavisinde siklofosfamidin ifosfamidin yerini alıp alamayacağını değerlendirdi ve VAC’nin (vinkristin, daktinomisin ve siklofosfamid) VAI’den (vinkristin, daktinomisin ve ifosfamid) istatistiksel olarak daha aşağıda olmadığını öne sürdü; ancak VAI, biraz daha yüksek 3 yıllık olaysız sağkalım EFS ile ilişkilendirildi. Çocuk Onkoloji Grubu’nun (COG) bir faz III çalışmasında (AEWS0031), hastalar her üç haftada bir IE ile dönüşümlü olarak VDC aldı. Çalışma, toksisiteyi arttırmadan 2 haftalık aralıkların 3 haftalık aralıklardan daha etkili olduğunu göstermiştir.
Bu sonuçlar, VDC/IE’nin Amerika Birleşik Devletleri’nde bakım standardı olmasına yol açtı. Kemoterapiye lokal tedaviden önce başlanır ve herhangi bir ilerleme belirtisi yoksa ameliyat sonrası devam edilir. Cerrahi rezeksiyon ve RT lokal kontrol tedavi yaklaşımlarıdır. Bugüne kadar bu iki yaklaşımın etkinliğini karşılaştıran hiçbir çalışma bulunmamaktadır. INT-0091 çalışması, tek başına cerrahi ile tek başına RT arasında lokal başarısızlık veya olaysız sağkalım açısından anlamlı farklar bulamadı. Ancak cerrahi artı RT’nin daha düşük lokal başarısızlık insidansı ile ilişkili olduğu bulunmuştur. Buna rağmen cerrahi olarak tedavi edilmeden sadece RT verilen olgularda hastalık nüksünün kaçınılmaz olduğu kanaatindeyiz. CESS 81, CESS 86 ve EICES-92 çalışmalarından elde edilen 1058 hastanın verileri, cerrahi+RT ve sadece cerrahinin, sadece RT’ye göre önemli ölçüde daha düşük lokal başarısızlık oranına sahip olduğunu gösterdi. Lokal başarısızlık insidansı ameliyat öncesi RT grubunda ve ameliyat sonrası RT olan veya olmayan cerrahi grupta benzerdi. INT-0091, INT-0154 veya AEWS0031 çalışmalarına kayıtlı hastalardan elde edilen veriler ışığında cerrahi+RT’nin sadece RT’ye göre daha düşük lokal başarısızlık riski ile ilişkili olduğunu gösterildi.
2. Kondrosarkom
Kondrosarkom Tedavisi: Kondrosarkom Belirtileri:
Kondrosarkom Nedir?
Kondrosarkom, kıkırdak hücrelerinden gelişen bir tür kemik kanseridir. Kıkırdak yetişkinlerde bulunan ve çoğu kemiğin geliştiği doku olan özelleşmiş bağ dokusudur. Kıkırdak büyüme sürecinde önemli bir rol oynar. Vücutta birçok farklı kıkırdak türü mevcuttur. Kondrosarkom öncelikle femur (uyluk kemiği), kol, pelvis veya dizdeki kıkırdak hücrelerini etkiler. Daha az sıklıkta olsa da diğer alanlar da (kaburgalar gibi) etkilenebilir. Kondrosarkom, primer kemik kanserinin ikinci en sık görülen türüdür. Birincil kemik kanseri kemikten başlayan kanserdir. Bu kanser türü 20 yaşın altındaki bireyleri nadiren etkiler. Risk 75 yaşına kadar artmaya devam eder. Kadın ve erkek arasındaki görülme sıklığı eşittir.
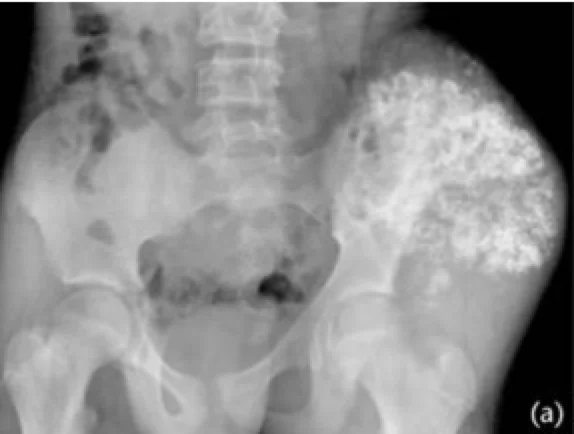
Kondrosarkomun Nedeni Nedir?
Kondrosarkomun kesin nedeni bilinmemektedir. Bazı bireyleri bu tür malignitelere daha açık hale getiren genetik veya kromozomal bir bileşen olabilir. Kondrosarkomlar diğer kanserlere yönelik radyasyon tedavisinin geç bir sonucu olarak gözlemlenmiştir.
Kondrosarkom İçin Risk Faktörleri Nelerdir?
Çoğu zaman kondrosarkom normal kıkırdak hücrelerinden kaynaklanır. Ayrıca önceden var olan iyi huylu (kanserli olmayan) bir kemik veya kıkırdak tümöründen de kaynaklanabilir. Aşağıda kondrosarkom meydana geldiğinde mevcut olabilecek bazı iyi huylu durumların bir listesi bulunmaktadır:
- Enkondromlar. Kıkırdaktan başlayan ve genellikle elleri etkileyen (diğer bölgeleri de etkileyebilen) bir tür iyi huylu kemik tümörü.
- Çoklu ekzostozlar (osteokondromlar). Çoklu osteokondromların varlığı
- Ollier hastalığı. Bir grup enkondrom (genellikle elleri etkileyen iyi huylu kıkırdak tümörleri).
- Maffucci sendromu. Çoklu enkondromların (genellikle elleri etkileyen iyi huylu kıkırdak tümörleri) ve anjiyomların (kan damarlarından oluşan iyi huylu tümörler) birleşimi.
Kondrosarkomun Belirtileri Nelerdir?
Kondrosarkom belirtileri tümörün konumuna bağlı olarak değişebilir. Aşağıdakiler kondrosarkomun en sık görülen semptomlarıdır. Ancak her bireyde belirtiler farklı şekilde ortaya çıkabilir. Belirtiler şunları içerebilir:
- Etkilenen kemikte büyük kitle
- Kitle etrafında basınç hissi
- Zamanla yavaş yavaş artan ağrı. Genellikle geceleri daha da kötüleşir ve ibuprofen gibi antiinflamatuar ilaçlar alınarak hafifletilebilir. Genellikle dinlenmeyle rahatlamaz.
- Yerel şişlik
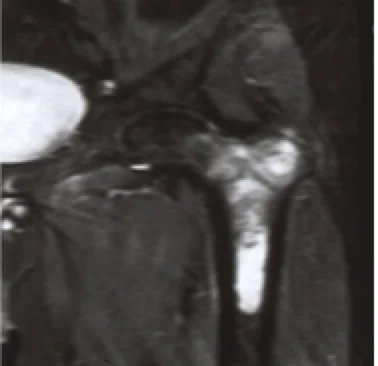
Kondrosarkom Nasıl Teşhis Edilir?
Tam bir tıbbi öykü ve fizik muayeneye ek olarak, kondrosarkom için teşhis prosedürleri aşağıdakileri içerebilir:
- Röntgen. İç dokuların, kemiklerin ve organların görüntülerini filme dönüştürmek için görünmez elektromanyetik enerji ışınlarını kullanan bir tanı testidir.
- Bilgisayarlı tomografi taraması (CT veya CAT taraması da denir). Bu, vücudun ayrıntılı görüntülerini oluşturmak için X ışınlarını ve bilgisayarı kullanan bir görüntüleme testidir. CT taraması kemiklerin, kasların, yağların ve organların ayrıntılarını gösterir.
- Manyetik rezonans görüntüleme (MRI). Vücuttaki organların ve yapıların ayrıntılı görüntülerini almak için büyük mıknatıslar, radyofrekanslar ve bilgisayar kombinasyonunun kullanıldığı bir teşhis prosedürü.
- Pozitron emisyon tomografisi (PET) taraması. Radyoaktif etiketli glikozun (şeker) kan dolaşımına enjekte edildiği bir görüntüleme testi. Glikozu normal dokulardan daha fazla kullanan dokular (tümörler gibi) bir tarama makinesi tarafından tespit edilebilir.
- Biyopsi. Mikroskop altında incelenmek üzere vücuttan doku örneklerinin (iğneyle veya ameliyat sırasında) alındığı bir prosedür. Bu, kanser veya diğer anormal hücrelerin mevcut olup olmadığını belirlemek için yapılır.
Kondrosarkom Tedavisi:
Kondrosarkomun özel tedavisi sağlık uzmanınız tarafından aşağıdakilere göre belirlenecektir:
- Yaşınız, genel sağlığınız ve tıbbi geçmişiniz
- Kanserin türü, evresi (yayımı) ve yeri
- Belirli ilaçlara, prosedürlere ve terapilere karşı toleransınız
- Hastalığın seyrine ilişkin beklenti
- Fikriniz veya tercihiniz
Kondrosarkom tedavisinin amacı kitleyi çıkarmak ve geri dönme olasılığını azaltmaktır. Tedavi şunları içerebilir:
- Ameliyat. Tümörün çıkarılması. Tümör bir kol veya bacaktaysa cerrah uzvu kurtarmaya çalışacaktır. Bazı durumlarda amputasyona ihtiyaç duyulabilir.
- Fizik Tedavi. Bu tedavi, ameliyattan sonra etkilenen bölgenin gücünü ve kullanımını yeniden kazanmaya yardımcı olur.
- Radyasyon tedavisi. Radyasyon yüksek dozlarda verilebilir.
- Kemoterapi. Birincil tedavi olmasa da kanserin vücudun diğer bölgelerine yayılması durumunda buna ihtiyaç duyulabilir.
3. Osteosarkom
Osteosarkom Nedir?
Osteosarkom (OS) veya osteojenik sarkom (OGS) (veya kısaca kemik kanseri), kemikteki kanserli bir tümördür. Spesifik olarak, mezenkimal kökenli ilkel transforme hücrelerden kaynaklanan, osteoblastik farklılaşma sergileyen ve malign osteoid üreten agresif bir malign neoplazmdır. Osteosarkom, primer kemik sarkomunun en sık görülen histolojik formudur. En çok gençler ve genç yetişkinlerde görülür.
Osteosarkom Belirtileri:
Birçok hasta ilk olarak geceleri daha kötüleşen, aralıklı ve değişken yoğunlukta olabilen ve uzun süredir devam eden ağrıdan şikayetçidir. Sporla aktif olarak ilgilenen gençler sıklıkla uyluk kemiğinin alt kısmında veya dizin hemen altında ağrıdan şikayet ederler. Tümör büyükse, belirgin lokalize şişlik olarak ortaya çıkabilir. Bazen ani bir kırılma ilk semptom olabilir çünkü etkilenen kemik normal kemik kadar güçlü değildir ve küçük bir travma ile anormal şekilde kırılabilir. Pelvisten kaynaklananlar gibi cilde çok yakın olmayan daha derin yerleşimli tümörlerde lokalize şişlik belirgin olmayabilir.
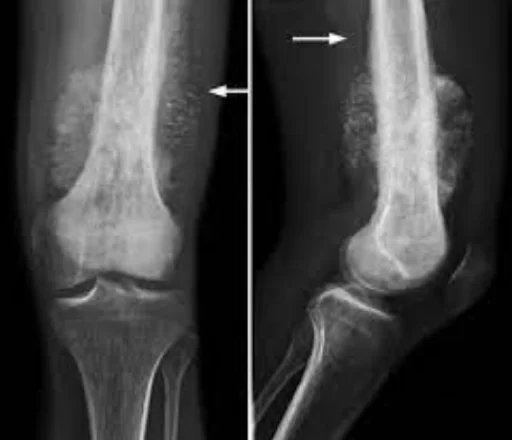
Osteosarkom Nedenleri:
13q14 kromozomunun silinmesinin retinoblastoma genini inaktive ettiği ailesel vakalar, yüksek osteosarkom gelişimi riski ile ilişkilidir. Paget kemik hastalığı, fibröz displazi, enkondromatozis ve kalıtsal çoklu ekzostozları içeren kemik displazileri osteosarkom riskini artırır.
Li-Fraumeni sendromu (germline TP53 mutasyonu), osteosarkom gelişimi için predispozan bir faktördür. Rothmund-Thomson sendromu (yani konjenital kemik defektleri, saç ve deri displazileri, hipogonadizm ve kataraktın otozomal resesif ilişkisi) bu hastalığın artan riskiyle ilişkilidir. Sr-90’ın yüksek dozları, hayvanlarda kemik kanseri ve lösemi riskini artırıyor ve insanlarda da bunu yaptığı tahmin ediliyor.
Florür Osteosarkom Yapar mı?
Suyun florlanması ile kanser veya kansere bağlı ölümler arasında, hem genel olarak kanser hem de özellikle kemik kanseri ve osteosarkom için açık bir ilişki yoktur. Bir dizi araştırma, sudaki florür konsantrasyonunun osteosarkomla ilişkili olmadığı sonucuna vardı. Florüre maruz kalma ve osteosarkom ilişkisine ilişkin inanışlar, 1990 yılında ABD Ulusal Toksikoloji programında yapılan ve erkek sıçanlarda florür ile osteosarkom ilişkisine dair belirsiz kanıtlar gösteren bir çalışmadan kaynaklanmaktadır. Ancak florürün farelerde kansere neden olma eğilimine dair hala sağlam bir kanıt bulunmuyor. Vatandaşların diş sağlığını iyileştirmek için dünya çapında suyun florlanması uygulanmaktadır. Aynı zamanda büyük bir sağlık başarısı olarak kabul edilir. Su kaynaklarındaki florür konsantrasyon seviyeleri, Amerika Birleşik Devletleri Çevre Koruma Ajansı’nın florür seviyelerini litre başına 4 miligramdan fazla olmayacak şekilde düzenlemesi gibi düzenlenir. Aslında su kaynaklarında zaten doğal olarak oluşan florür bulunmaktadır, ancak birçok topluluk diş çürümesini azaltabileceği noktaya kadar daha fazla florür eklemeyi tercih etmiştir. Florürün aynı zamanda yeni kemik oluşumuna neden olma özelliği ile de bilinmektedir. Ancak daha ileri araştırmalar, insanlarda florürlü suyun osteosarkom riski taşımadığını göstermektedir. Araştırmaların çoğu, içme suyunda farklı florür konsantrasyonlarına sahip belirli bölgelerdeki osteosarkom hastalarının sayısının sayılmasını içeriyordu. Verilerin istatistiksel analizi farklı florürlü bölgelerdeki osteosarkom vakalarının görülme sıklığında anlamlı bir fark olmadığını göstermektedir. Bir diğer önemli araştırma, florür konsantrasyonunu ölçmek ve bunları yeni teşhis edilen kötü huylu kemik tümörlerinin kemik örnekleriyle karşılaştırmak için osteosarkom hastalarından kemik örnekleri toplamayı içeriyordu. Sonuç, osteosarkom hastalarının ve tümör kontrollerinin kemik numunelerindeki ortalama florür konsantrasyonlarının anlamlı derecede farklı olmadığıdır. Sadece kemiklerdeki florür konsantrasyonunun değil, aynı zamanda osteosarkom hastalarının florür maruziyetinin de sağlıklı insanlardan önemli ölçüde farklı olmadığı kanıtlanmıştır.
Osteosarkom kemik büyümesi bölgelerinde ortaya çıkma eğilimindedir; bunun nedeni muhtemelen çoğalmanın bu bölgedeki osteoblastik hücreleri, hücrelerin dönüşümüne yol açabilecek mutasyonlar kazanmaya yatkın hale getirmesidir (RB geni ve p53 geni). Tümör uzun kemiğin ucunda (genellikle metafizde) lokalize olabilir. Çoğu zaman tibia veya humerusun proksimal ucunu veya femurun distal ucunu etkiler. Osteosarkom vakaların %60’ında diz çevresindeki bölgeleri, %15’i kalça çevresini, %10’u omuzu ve %8’i çeneyi etkileme eğilimindedir. Tümör, kalsifiye kemikteki tümör spiküllerinin dik açılarla yayılması nedeniyle (röntgen muayenesinde “köknar ağacı”, “güve yeniği” veya “gün batımı ” görünümü) katı, sert ve düzensizdir. Bu dik açılar, Codman üçgeni olarak bilinen şeyi oluşturur; bu, osteosarkomun karakteristik özelliğidir ancak tanısal özelliği değildir.
Osteosarkom Teşhis:
X ışınları, osteosarkomu teşhis etmek için tercih edilen ilk görüntüleme yöntemidir. Osteosarkomun röntgen filmlerindeki bazı özellikleri gün batımı görünümü ve Codman üçgenidir (yeni kemik oluşumuna neden olan tümörün kemik korteksinin yükselmesi). BT taraması, kemik anatomisinin, kemik korteksinin bütünlüğünün tanımlanmasında, patolojik kırığın tespit edilmesinde ve ossifikasyonun (yeni kemik materyallerinin döşenmesi) ve kıkırdak kalsifikasyonunun değerlendirilmesinde faydalıdır. Öte yandan yumuşak doku ve medüller kavite MR taramasıyla daha iyi görüntülenmektedir.
Şüpheli osteosarkomun biyopsisi kalifiye bir ortopedik onkolog tarafından yapılmalıdır. Amerikan Kanser Derneği şunu belirtiyor: “Muhtemelen başka hiçbir kanser vakasında bu prosedürün doğru şekilde uygulanması bu kadar önemli değildir. Uygunsuz şekilde yapılan bir biyopsi, etkilenen uzuvun amputasyondan kurtarılmasını zorlaştırabilir.” Ayrıca akciğerlere de metastaz yapabilir ve esas olarak göğüs röntgeninde alt bölgelerde tek veya çoklu yuvarlak nodüller şeklinde görünebilir.
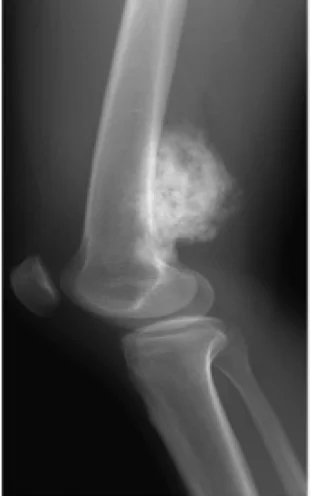
Osteosarkom Tipleri:
- Konvansiyonel: osteoblastik, kondroblastik, fibroblastik
- Telenjiektatik
- Küçük hücreli
- Düşük dereceli merkezi
- Periosteal
- Paraosteal
- İkincil
- Yüksek dereceli yüzey
- İskelet dışı
Osteosarkom Tedavisi:
Osteosarkomda kanserin tam cerrahi, en blok rezeksiyonu tercih edilen tedavi yöntemidir. Her ne kadar çoğu hasta uzuv kurtarma ameliyatı geçirebilse de, komplikasyonlar (özellikle enfeksiyon, protez gevşemesi ve kaynamama veya lokal tümör nüksü) daha ileri cerrahi veya ampütasyon ihtiyacını doğurabilir.
OSTEOSARKOMLU HASTALAR EN İYİ ŞEKİLDE SARKOM TEDAVİSİNDE DENEYİMLİ BİR ORTOPEDİK ONKOLOG TARAFINDAN YÖNETİLİR. Mevcut standart tedavi neoadjuvan kemoterapi (ameliyattan önce verilen kemoterapi) ve ardından cerrahi rezeksiyondur. Ameliyattan sonra tümörde görülen tümör hücresi nekrozunun (hücre ölümü) yüzdesi prognoz hakkında fikir verir ve aynı zamanda onkoloğun ameliyattan sonra kemoterapi rejiminin değiştirilmesi gerekip gerekmediğini bilmesini sağlar.
Standart tedavi, mümkün olduğunda uzuv kurtarıcı ortopedik cerrahi (veya bazı durumlarda amputasyon) ve yüksek doz metotreksat ile lökovorin kurtarma, intraarteriyel sisplatin, adriamisin, ifosfamid ile mesna, BCD (bleomisin, siklofosfamid, daktinomisin) etoposid ve muramil tripeptit kombinasyonudur. Kullanılan protokol, tedaviyi arteriyografik cevaba göre kişiselleştiren agresif bir intra-arteriyel rejimdir. Bazı çalışmalarda üç yıllık olaysız sağkalım %50 ila %75 arasında değişirken, beş yıllık sağkalım %60 ila %85 arasında değişmektedir. Genel olarak, beş yıl önce tedavi edilen hastaların %65-70’i bugün hayatta olacaktır. Bu hayatta kalma oranları genel ortalamalardır ve bireysel nekroz oranına bağlı olarak büyük ölçüde değişiklik gösterir.
Osteosarkom Hastalığın Seyiri:
Grade I osteosarkom nadirdir ve parosteal osteosarkom ve düşük dereceli santral osteosarkomu içerir. Geniş rezeksiyonla mükemmel bir prognoza (>%90) sahiptir. Genel prognoz tümörün konumuna (proksimal tibia, femur, pelvis vb.), tümör kitlesinin boyutuna ve neoadjuvan kemoterapiden kaynaklanan nekrozun derecesine bağlıdır. P-glikoproteinin derecesi, tümörün cxcr4-pozitif veya Her2-pozitif olup olmadığı gibi diğer patolojik faktörler de önemlidir, çünkü bunlar akciğere uzak metastazlarla ilişkilidir. Osteosarkom nedeniyle ölüm oranları yılda yaklaşık %1,3 oranında azalmaktadır. Osteosarkom için uzun vadeli hayatta kalma olasılıkları 20. yüzyılın sonlarında önemli ölçüde iyileşti ve 2009’da yaklaşık %68’e ulaştı.




